No reino da ficção científica, partes do corpo eletrônicos são chapéu velho. Mas para os seres humanos de carne e sangue, os avanços nessa área estão alterando rapidamente as perspectivas para o coração tratamento avançado fracasso. Embora as inovações na terapia medicamentosa transformaram o curso da insuficiência cardíaca precoce e moderada, a forma avançada da doença continua a ser um problema médico obstinado. No entanto, a mesma tecnologia eletrônica do século 21 que nos traz telefones celulares cada vez mais compactos e players de música mais minúsculo está a ser aproveitada para produzir uma matriz de menor, mais leve, e aparelhos mais sofisticados para auxiliar o coração doente. Que vão desde o tamanho de um baralho de cartas para um par de libras, essas máquinas em miniatura são capazes de reproduzir muitas das funções elétricas e mecânicas do coração natural.
Ventricular dispositivo auxiliar
Um coração artificial? Não é bem assim, mas a mais nova geração de dispositivos de assistência ventricular (VADs) está caminhando nessa direção. A DVA é uma bomba acionada por bateria implantado no peito para apoiar a ação de bombeamento de um ou ambos os ventrículos. Os criadores dos primeiros VADs na década de 1970 viu estes dispositivos como uma potencial alternativa de longo prazo para transplante de coração. Esta visão só agora está sendo realizado. Enquanto isso, VADs ter assegurado um lugar importante em outros aspectos de cuidados cardíacos.
O primeiro uso de um VAD foi como uma recuperação da ponte-to-, para ajudar o coração de uma pessoa se recuperar depois de um ataque cardíaco ou outro dano cardíaco. VADs assumiu progressivamente um segundo papel como ponte para o transplante - uma medida provisória para manter um candidato ao transplante vivo até que um doador estava disponível. O entusiasmo atual sobre VADs, no entanto, concentra-se em sua aplicação crescente como uma opção de tratamento prolongado para pessoas com estágio final da insuficiência cardíaca, chamada de terapia de destino. Um ensaio de referência, publicado no The New England Journal of Medicine, em 2001, foi o primeiro estudo a demonstrar que, em comparação com as formas existentes de terapia médica, VADs ventrículo esquerdo pode oferecer melhores chances de sobrevivência para pessoas com insuficiência cardíaca em fase terminal que não estivessem ' t candidatos para transplante. Com base nesses resultados, a pesquisa em curso pretende direcionar melhor os pacientes que podem se beneficiar do procedimento. O aparelho em si está evoluindo bem. VADs mais novos são menores e operam com uma ação de bombeamento mais sofisticado do que os modelos anteriores (ver Figura 9).
Apesar da promessa oferecida por VADs, a taxa de sucesso da vida real é modesto. Infecção e de outras complicações sérias podem resultar a partir da implantação. Por causa destes riscos, VADs são atualmente consideradas apenas para os indivíduos gravemente doentes que já tenham corações criticamente comprometidos. Como as perspectivas para a sobrevivência a longo prazo com um VAD continua a iluminar, pode ser razoável para oferecer esta tecnologia a um espectro mais amplo de pessoas.
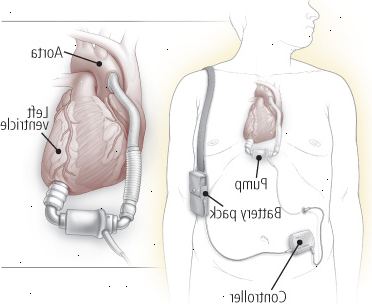
Figura 9: ventricular dispositivo auxiliar (VAD)
Um dispositivo de assistência ventricular (DAV) ajuda a bombear sangue do ventrículo enfraquecido. Mais apoiar o ventrículo esquerdo e são conhecidos como LVADs; recebem sangue do ventrículo esquerdo e entregá-lo para a aorta, como mostrado acima. Direito dispositivos de assistência ventricular (RVADs) recebem sangue do ventrículo direito e entregá-lo para a artéria pulmonar. VADs consistem de uma bomba, um sistema de controle, e uma fonte de energia. A bomba pode ser localizado dentro ou fora do corpo, enquanto que o sistema de controlo e fornecimento de energia se encontram fora do corpo. |
Coração totalmente artificial
A bomba mecânica auto-suficiente que pode levar mais para o coração por tempo indeterminado foi um sonho dos inventores médicos para a melhor parte de uma geração. Ao contrário de um VAD que suporta a acção do ventrículo esquerdo ou direito, um coração artificial substitui a função de ambos os ventrículos e é implantado no local do coração natural, o qual é removido durante o processo.
Talvez a primeira tentativa mais conhecida em um coração totalmente artificial foi o Jarvik-7, lançado em 1982. Este dispositivo consiste de uma bomba acionada pelo ar que operava a partir de um console de alimentação externa. O herdeiro moderno para o Jarvik-7, o CardioWest temporária Coração Artificial Total, é aprovado pelo FDA para uso como um transplante de bridge-to-para pessoas que sofrem de insuficiência cardíaca biventricular.
Outra entrada no campo é a substituição coração AbioCor implantável. Este dispositivo é constituído por uma bomba de duas libras implantado no peito e um controlador de bateria interna e que estão colocados no abdómen. A bateria pode ser recarregada através da pele a partir de uma fonte de alimentação externa. Isto permite que o paciente se mover livre de fios de cerca de duas horas de cada vez, tornando-se o coração artificial somente completamente auto-contido. O AbioCor garantiu aprovação limitada para uso em pessoas que não são elegíveis para transplante de coração e têm menos de um mês para viver de outra forma.
Cardioversor-desfibrilador implantável
O curso natural da insuficiência cardíaca tem um dos dois finais. Um indivíduo pode, eventualmente, morrer de um problema chamado falha da bomba, quando o coração torna-se tão fraco que não bombeia. O outro cenário freqüente é a morte súbita cardíaca devido a um batimento cardíaco irregular ou descontroladamente rápido no ventrículo, com contrações do coração ineficazes. Uma vez que este ritmo anormal toma conta, a única maneira de corrigi-lo é através da administração de um choque de energia elétrica para o músculo cardíaco para chocar-lo de volta em um ritmo normal. Apenas cinco em cada 100 pessoas que têm um desses episódios sobreviver o tempo suficiente para chegar ao hospital.
Coração arritmias são predominantes entre as pessoas com insuficiência cardíaca. Danos ao músculo cardíaco, especialmente após um ataque cardíaco, podem interferir com as vias de condução elétrica através do músculo. O problema é agravado pelo fato de que a maioria das drogas rotineiramente usados para estabilizar os ritmos irregulares também diminuir a força de contração do coração, um efeito colateral incompatível para as pessoas cujos corações já são fracos.
Na década de 1980, os médicos testaram um conceito revolucionário - um dispositivo em miniatura implantado no peito que iria sentir um ritmo anormal e entregar imediatamente um choque elétrico (ver Figura 10). Este foi o primeiro cardioversor-desfibrilador implantável (CDI). Desde então, as unidades tornaram-se menores, mais complexa e mais eficiente em termos de energia, levando a sua utilização generalizada.
Muitos ensaios clínicos avaliaram como CDIs levantar-se contra o tratamento medicamentoso tradicional em uma variedade de populações. Um estudo avaliou o desempenho notável de CDIs em pessoas que sofreram um ataque cardíaco e teve uma fração de ejeção do ventrículo esquerdo baixa - um marcador de insuficiência cardíaca. A taxa de mortalidade entre as pessoas pertencentes ao grupo ICD foi 31% menor do que no grupo que recebeu terapia medicamentosa. Este resultado foi tão esmagadoramente positiva que os investigadores pararam o estudo mais cedo. Além disso, os participantes de ambos os grupos estavam recebendo terapia medicamentosa ideal para a insuficiência cardíaca, o que demonstra que o ICD produziu benefícios para além dos resultantes da medicação. Em contrapartida, as pessoas que têm um ICD se queixam de que ele pode ser doloroso quando o dispositivo incêndios. Eles descrevem a sensação como um choque súbito similar ao que está sendo chutado no peito.
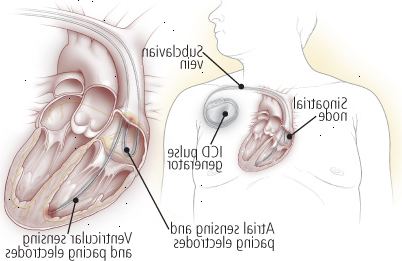
Figura 10: desfibriladores cardíacos implantáveis
Um desfibrilador cardíaco implantável (CDI) detecta anormais, ritmos cardíacos potencialmente mortais e corrige o ritmo defeituoso automaticamente. Para a inserção, o que é feito sob anestesia local, o cirurgião coloca eléctrodos no coração do paciente através de um dos grandes veias no peito. Depois de testar a colocação do eléctrodo, um pequeno gerador é colocado sob a pele, no peito. Se e quando este dispositivo detecta um ritmo anormal, o ICD restaura ritmo normal do coração, seja através da apresentação de um choque para o músculo cardíaco ou usando sinais de baixa energia repetidas (de estimulação cardíaca). O dispositivo também grava quando ocorrem ritmos anormais e quando choques são administrados. |
Terapia de ressincronização cardíaca
Pessoas com insuficiência cardíaca avançada, por vezes, estão sujeitos a danos às suas células de condução elétrica que causa um batimento cardíaco lento. Estas anomalias aparecem como padrões distintos sobre traçados de ECG e pode ser corrigido com um marca-passo de um padrão de chumbo ou um dispositivo dual-liderança que estimula tanto o átrio direito eo ventrículo direito. No entanto, as evidências sugerem que estas técnicas não são eficazes em pessoas com insuficiência cardíaca sistólica que têm um ventrículo esquerdo mal bombeamento. No ritmo normal de duas fases, o lado esquerdo contrai uma fração de segundo depois do que o direito. Estimular apenas o lado direito do coração perturba a coordenação natural dos dois sistemas de bombeamento, uma doença chamada assincronia ventricular. Este problema pode ser superado por adição de uma terceira vantagem do dispositivo que estimula o ventrículo esquerdo. O ritmo é sincronizado de modo que o ventrículo esquerdo recebe o sinal para contrair um pouco mais tarde do que o direito. Esta técnica é chamada de terapia de ressincronização cardíaca (CRT) ou estimulação biventricular.
Um estudo distribuídos aleatoriamente 813 pessoas com insuficiência cardíaca moderada a grave para obter CRT e terapêutico ou terapia médica sozinho. Aqueles que receberam CRT tiveram um menor risco de hospitalização ou morte por qualquer causa em comparação com a medicação só grupo.
Outra observação interessante a partir da avaliação desses dispositivos é que CRT pode realmente reverter alguns dos danos ventricular em pessoas com insuficiência cardíaca. As mudanças nas dimensões das câmaras de bombeamento, menos refluxo de sangue através da válvula mitral, e da redução da espessura da parede do ventrículo esquerdo todos fornecem evidência de um músculo cardíaco mais forte. Aproximadamente 20% a 40% das pessoas com insuficiência cardíaca Fase C poderiam ser candidatos para esta terapia.
Ressincronização cardíaca com ICD
Embora os resultados dos estudos iniciais de terapia de ressincronização cardíaca foram animadores, os pesquisadores notaram uma omissão importante. A taxa de mortalidade por morte súbita cardíaca permaneceu a mesma ou melhorou apenas ligeiramente. Uma vez que muitas pessoas com insuficiência cardíaca estão sujeitos a tanto batimento cardíaco lento e ventrículo esquerdo arritmias, o conceito de combinar as duas funções em um único dispositivo foi idealizada. Um estudo que avaliou o dispositivo combinado mostraram melhorias na taxa de morte súbita cardíaca. Quando acoplado com informações de outros estudos que avaliaram a eficácia dos CDIs, os benefícios são notáveis.
Monitores hemodinâmicos implantáveis
Out-of-control acúmulo de líquido é o coração falha complicação que na maioria das vezes envia pessoas para o hospital. Neste momento, a melhor forma os indivíduos podem medir seus níveis de fluido é pesar-se diariamente. Mas o sangue começa a acumular-se no coração e aumentar a pressão dentro dos ventrículos muito antes de peso corporal de uma pessoa altera visivelmente. Ter acesso a essas informações permitiria um médico para tomar medidas para corrigir o problema antes que ele se transforma em uma crise. Vários dispositivos atualmente em desenvolvimento são projetados para fazer exatamente isso.
Num tal dispositivo, um monitor hemodinâmica implantável é colocado sob a pele do seu peito por um procedimento similar ao de uma inserção de um pacemaker. A liderança de detecção de pressão liga o monitor ao átrio direito. As medições são armazenadas no monitor até que eles são baixados e transmitidos eletronicamente a um site central.
Em um estudo de 274 pacientes que usam o dispositivo, dias hospitalares totais caíram 21% durante um período de seis meses. Pessoas com insuficiência cardíaca classe funcional III saíram melhor do que aqueles com classe IV. Mesmo que o resultado da pesquisa aponta em uma direção positiva, os resultados não foram estatisticamente significativos. Isso levou circulatório Painel da FDA dispositivos do sistema de voto março 2007 contra a aprovação do dispositivo para a venda. O fabricante espera melhorar os resultados e liberar o monitor no futuro.
Transplante de coração
Uma vez considerado arriscado e experimental, o transplante cardíaco é hoje considerado o tratamento de escolha para muitas pessoas com insuficiência cardíaca grave. O destinatário do primeiro transplante de coração humano, realizada em 1967, sobreviveu por apenas 18 dias. Desde então, os avanços em medicamentos, técnicas cirúrgicas, e seleção de doadores resultaram em avanços notáveis no campo. Desde o início de 1980, a taxa de sobrevivência de um ano depois de um transplante de coração subiu de menos de 70% para cerca de 85% a partir de 2006. E cerca de 70% dos receptores de transplante cardíaco sobrevivem cinco anos.
O maior avanço no sucesso do transplante veio em 1983 com a introdução da ciclosporina. Esta medicação potente suprime o sistema imunológico, impedindo assim a rejeição do tecido, uma das principais complicações na sequência de um transplante de órgão. Os medicamentos similares são agora um padrão em cuidados pós-transplante. Além disso, os médicos aprenderam como melhor identificar e tratar outros riscos importantes após o transplante, incluindo a infecção que resulta de amortecimento do sistema imunológico ea doença vascular que, por vezes, desenvolve-se em artérias que alimentam o coração do doador.
Outra tecnologia emergente tem o potencial para melhorar ainda mais as taxas de sucesso de transplantes. Um programa piloto em curso em cinco principais centros de transplante está avaliando um sistema que mantém o coração em um estado de funcionamento, como é transportado do doador ao receptor. Porque o coração continua batendo, o fornecimento de sangue e oxigênio para o órgão permanece constante. Isto pode, potencialmente, limitar os danos de tecidos durante o tempo que o coração está fora do corpo e, finalmente, reduzir o risco de rejeição, uma vez que é reimplantado. Mais de 2.000 transplantes de coração são realizados anualmente na Europa. No entanto, há muito menos corações de doadores que não são candidatos elegíveis. Pelo menos o dobro de pessoas poderiam se beneficiar do procedimento se mais órgãos disponíveis.